在做代谢组学分析的时候,经常会听到QC,QC是样本检测过程中必不可少的一部分,可用于考察方法的稳定性和重复性,今天给大家分享一篇QC的科普贴。如有疑问和不足,欢迎留言
QC样本的制备
:
-
混合
相同体积
的所有待检测样本,然后按照与待测样本相同的前处理方法来处理QC样本,之后进样进行LC-MS分析。 -
样本检测时,通常在检测最开始运行几次QC样本,之后根据样本量的大小在每检测几个样本之后检测一次QC样本。
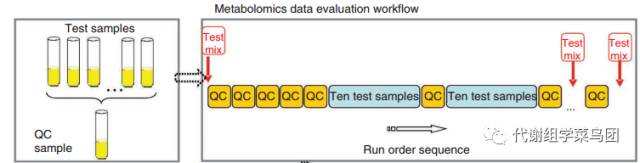
(图片来源:Want E J, Wilson I D, Gika H, et al. Global metabolic profiling procedures for urine using UPLC–MS. Nature protocols, 2010, 5(6): 1005-1018.)
方法学考察
:
-
方法一:
-
最早使用的一种方法,从QC样本的总离子流图中选择具有代表性的离子峰(覆盖不同的保留时间,不同的强度),在对QC样本进行重复检测之后,计算这些离子的保留时间以及峰面积的相对标准偏差(RSD),用以考察分析方法的稳定性以及重复性。
-
方法二:
-
所有样品检测完之后,收集所有的QC样本的原始数据进行数据预处理,包括(峰提取,排列,归一化等),经过数据过滤(80%规则)之后,计算剩下的峰的峰面积的RSD值。
-
通常如果在
一个样本中有超过70%的化合物的RSD值小于等于30%
,则证明该方法有良好的稳定性以及重复性,所得到的数据可靠(也有不同的评价标准,比如要求
LC-MS数据小于20%
,
GC-MS数据小于30%
等)。
-
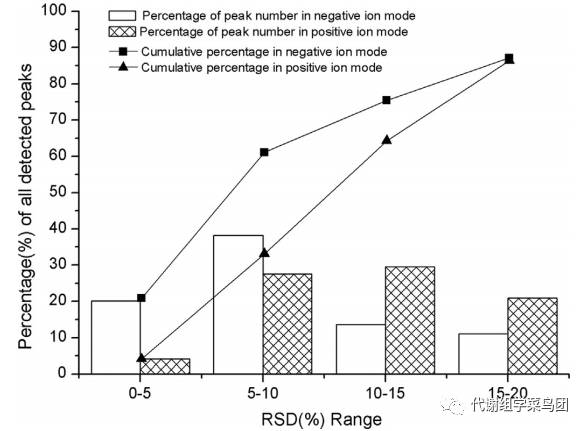
图中
柱形图
表示化合物在不同RSD范围内的
百分比分布
,
折线图
表示在不同RSD范围的
累计百分比
。
-
方法三:
-
原始数据经过数据预处理之后,将
所有样本(包括QC样本)
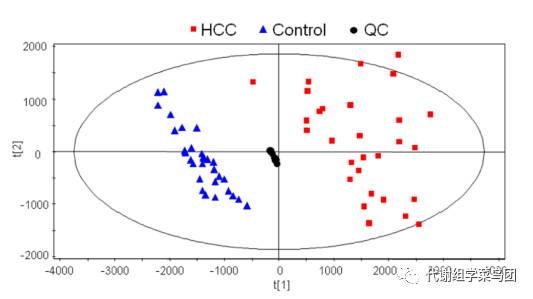
进行PCA分析,在得分图中观察QC样本的聚集程度。
-
由于QC样本是 等量混合了所有的被检测样本,理论上QC样本包含了所有样本中的代谢物,因此QC样本理论上会
分布在原点周围
。 -
图中QC样本
紧密聚集
,证明方法
稳定,重复性良好
。
-
方法四:
-
采用混合标准品作为QC,该QC通常包含
不同物理化学性质的体内和体外代谢物(使所选择的化合物具有代表性)
。 -
检测结束后,计算这些化合物的
保留时间以及峰面积的RSD
用以对分离分析方法进行评价。
参考文献
-
Want E J, Wilson I D, Gika H, et al. Global metabolic profiling procedures for urine using UPLC–MS. Nature protocols, 2010, 5(6): 1005-1018.
-
Dunn W B, Broadhurst D, Begley P, et al. Procedures for large-scale metabolic profiling of serum and plasma using gas chromatography and liquid chromatography coupled to mass spectrometry. Nature protocols, 2011, 6(7): 1060-1083.